Durch die Umwandlung von Plattenepithel in schmerzunempfindliches Zylinderepithel zeigt sich bei langjährigem Reflux oft keine klassische Symptomatik mehr. Dadurch erhöht sich das Risiko für eine Progression eines Barrett-Ösophagus. Das niedrige Risiko für die Entwicklung eines Karzinoms Jahr relativiert sich – berücksichtigt man den Akkumulationseffekt vor allem bei jüngeren Patienten.
Martin Schiller
Ein Screening auf einen Barrett-Ösophagus mittels Endoskopie sollte dann erfolgen, wenn der Betroffene mindestens fünf Jahre an einem Reflux leidet, über 50 Jahre alt ist und mindestens einen weiteren Risikofaktor wie etwa männliches Geschlecht, Kaukasier, Adipositas, Raucher, positive Familienanamnese für Barrett-Ösophagus oder Ösophagus-Karzinom aufweist. So ist es zumindest in den aktuellen Leitlinien vorgesehen. „Der hellhäutige Mann über 50 Jahre mit Übergewicht und einer Hiatus-Hernie mit häufigem nächtlichem Reflux wird als absoluter Risikopatient für den Barrett-Ösophagus eingestuft“, sagt Univ. Prof. Andreas Püspök, Vorstand der Abteilung für Innere Medizin II am Krankenhaus der Barmherzigen Brüder in Eisenstadt. Zu berück-sichtigen sei auch, dass nach Umwandlung des Plattenepithels in ein Zylinderepithel oftmals keine klassische Symptomatik mehr bestehe. „Das Zylinderepithel ist schmerzunempfindlich. Es kommt noch zu funktionellen Reflux-Beschwerden. Sie werden aber weniger stark wahrgenommen.“ Fällt der Schutzmechanismus Schmerz großteils weg, liegt auch ein Risikofaktor für ein unbemerktes Voranschreiten des Barrett-Ösophagus vor.
Die Prävalenz des Barrett-Ösophagus beträgt in der Allgemeinbevölkerung ein bis zwei Prozent. „Bezogen auf Personen mit Reflux schwanken die Zahlen zwischen zwei und 13 Prozent. In den Studien zeigt sich somit kein einheitliches Bild“, sagt Franziska Baumann-Durchschein von der Universitätsklinik für Innere Medizin an der Medizinischen Universität Graz. Bei 40 Prozent der Patienten entwickelt sich ein Barrett-Ösophagus ohne klassische Reflux-Symptome. Das Risiko für die Entstehung eines Ösophagus-Karzinoms beziffert die Expertin mit 0,3 Prozent pro Jahr, „sofern keine dysplastischen Areale bestehen“. Püspök macht trotz des geringen jährlichen Risikos auf den Akkumulationseffekt aufmerksam, „besonders wenn Personen jüngeren oder mittleren Alters die Diagnose erhalten“.
„… Risiko für Tumorentwicklung 0,3 Prozent pro Jahr …“ Franziska Baumann-Durchschein Medizinische Universität Graz
Ausdehnung bestimmt Kontrollen
Wurde in der Gastroskopie eine Barrett-Schleimhaut nachgewiesen, erfolgt eine ausgiebige Inspektion der Mukosa mit anschließender Biopsie der sus-pekten Areale sowie eine Vier-Quadranten-Biopsie alle ein bis zwei Zentimeter. „Diese Biopsie nach dem Seattle-Protokoll ist nach wie vor Standard“, betont Püspök. Liegt keine Dysplasie vor, richtet sich die Frequenz der endoskopischen Kontrollen nach der
Längenausdehnung:
- Short-Barrett-Ösophagus: Länge unter drei Zentimeter, Kontrolle alle fünf Jahre;
- Long-Barrett-Ösophagus: Länge mindestens drei Zentimeter, Kontrolle alle drei Jahre;
- Bei über zehn Zentimetern Länge wird eine jährliche Kontrolle empfohlen.
Ohne Vorliegen von dysplastischen Arealen soll eine Ablation laut den Leitlinien nicht erfolgen. „Je mehr Zeit man in die Inspektion der Mukosa inves-tiert, desto eher findet man aber doch ein dysplastisches Areal“, meint Püspök.
Chemoprävention umstritten
Hinsichtlich der medikamentösen Therapie des Barrett-Ösophagus ohne Dysplasie gibt es international unterschiedliche Ansichten. Baumann-Durchschein verweist auf die Deutschen Leitlinien, in denen nur eine an Reflux- Symptomen und begleitendenpeptischen Läsionen orientierte medikamentöse Therapie erfolgen sollte. „In diesen Leitlinien ist jedoch keine Chemoprävention zur malignen Entartung mit Protonenpumpenhemmern vorgesehen.“ Ein Barrett-Ösophagus wird demnach nicht als Indikation für eine Dauertherapie mit PPI angesehen. In den im Oktober 2023 aktualisierten Guidelines der European Society of Gastrointestinal Endoscopy (ESGE) hingegen wird die Standarddosis eines Protononenpumpeninhibitors zur Chemoprävention bei Patienten mit Barrett-Ösophagus vorgeschlagen, da es diesbezüglich eine steigende Evidenz gibt.
Der Empfehlungsgrad ist allerdings schwach. Verwiesen wird in der EGSE-Leitlinie auf die Ergebnisse der AspECT-Studie mit über 2.500 Patienten. Hier konnte gezeigt werden, dass die Kombination aus hochdosiertem PPI und Aspirin effektiv in der Verhinderung von ösophagealen Karzinomen oder der Entwicklung von hochgradigen Dysplasien ist (siehe Kasten). Eine Empfehlung zur Einnahme von Aspirin wurde daraus jedoch nicht abgeleitet. „Es gibt Hinweise, dass PPI ein Fortschreiten des Barrett-Ösophagus verhindern, konkrete Beweise fehlen jedoch. Daher sind Leitlinien zurückhaltend formuliert“, resümiert Baumann-Durchschein.
Keine Empfehlung sprechen beide Experten für eine Fundoplicatio als Barrett-Ösophagus-Therapie aus. „Es gibt keinen Beweis, dass die Anti-Reflux-Operation die Entstehung von Dysplasien oder Karzinomen besser verhindert als eine PPI-Therapie“, erklärt Püspök dazu. Die Fundoplicatio sei eine symptomatische Therapie, die besonders bei einer großen Hiatushernie mit Volumenreflux wirksam ist. Baumann-Durchschein weist darauf hin, dass bei bestehendem Barrett-Ösophagus ein Karzinom in der Gastroskopie schlechter erkennbar ist: „Durch die Fundusmanschette könnte ein Tumor eventuell übersehen werden.“
Kommt es zum Nachweis von Dysplasien im Barrett-Ösophagus, besteht ein hohes Progressionsrisiko. „Diese Fälle sollten an ein spezialisiertes Zentrum überwiesen werden“, betont Baumann-Durchschein. Das Vorliegen einer niedriggradigen Dysplasie muss stets von einem zweiten Pathologen bestätigt werden, da es sich häufig um eine Fehldiagnose handelt. Bei gesicherter Diagnose wird zwischen sichtbaren und nicht-sichtbaren Läsionen unterschieden. „Besteht keine sichtbare Läsion, wird entweder eine Radiofrequenzablation durchgeführt oder es erfolgt eine klinische Kontrolle in sechs Monaten, um eine visible lesion auszuschließen“, erklärt Baumann-Durchschein. Im Fall einer high-grade Dyplasie sei die Vorgangsweise ähnlich: Es werde zunächst nach einer sichtbaren Läsion gesucht und abgeklärt, ob eine endoskopische Abtragung erfolgen kann. Eine Resektion erfolgt bei Dysplasien mit sichtbaren Läsionen oder mukosalem Karzinom. Nach Resektion aller sichtbaren Dysplasien wird der nicht-dys-plastische Teil der Barrett-Mukosa in der Regel abliert.
Im Stadium der niedriggradigen Dysplasie werden mit der Radiofrequenzablation sehr gute Erfolge erzielt, sind sich die beiden Experten einig. „In rund 90 Prozent der Fälle kann die Barrett-Mukosa entfernt werden“, sagt Baumann-Durchschein. Püspök verweist zudem auf „längerfristig niedrige Rezidivraten“. Nach erfolgreicher Ablation einer low-grade Dysplasie sollte nach ein, drei und fünf Jahren eine erneute Gastroskopie erfolgen. Nach Abtragung einer high-grade Dysplasie wird empfohlen, Rezidivkontrollen nach ein, zwei, drei, vier, sieben und zehn Jahren durchzuführen. „Außerdem sollte nach jeder Ablation eine ein- bis zweijährige Therapie mit Protonenpumpeninhibitoren erfolgen, um eine gute Abheilung zu gewährleisten“, rät Baumann-Durchschein.
„… niedrige Rezidivraten nach Radiofrequenzablation …“ Univ. Prof. Andreas Püspök Barmherzige Brüder Eisenstadt
AspECT-Studie: 40 mg PPI effektiv
In der AspECT-Studie erhielt ein Teil der 2.557 Barrett-Ösophagus-Patienten zweimal täglich 40 Milligramm eines PPI und ein Teil des Kollektivs eine niedrigere Dosis von 20 Milligramm eines PPI, jeweils mit und ohne Aspirin. Der Beobachtungszeitraum betrug (im Median) 8,9 Jahre. Primärer Endpunkt der Studie war die Gesamtsterblichkeit oder die Entwicklung einer hochgradigen Dysplasie oder eines ösophagealen Adenokarzinoms. Die Einnahme des hochdosierten PPI mit Aspirin erwies sich in der Reduktion der Endpunkte effektiver als die Einnahme des niedrig dosierten PPI ohne Aspirin. Unterschiede zwischen den Schemata mit und ohne Aspirin waren statistisch allerdings nicht signifikant. In der ESGE-Leitlinie wird auf das Fehlen einer Gruppe ohne PPI-Einnahme und auf den kombinierten Endpunkt Gesamtsterblichkeit verwiesen. Abschließende Empfehlungen zur Chemoprävention werden daher nicht ausgesprochen.
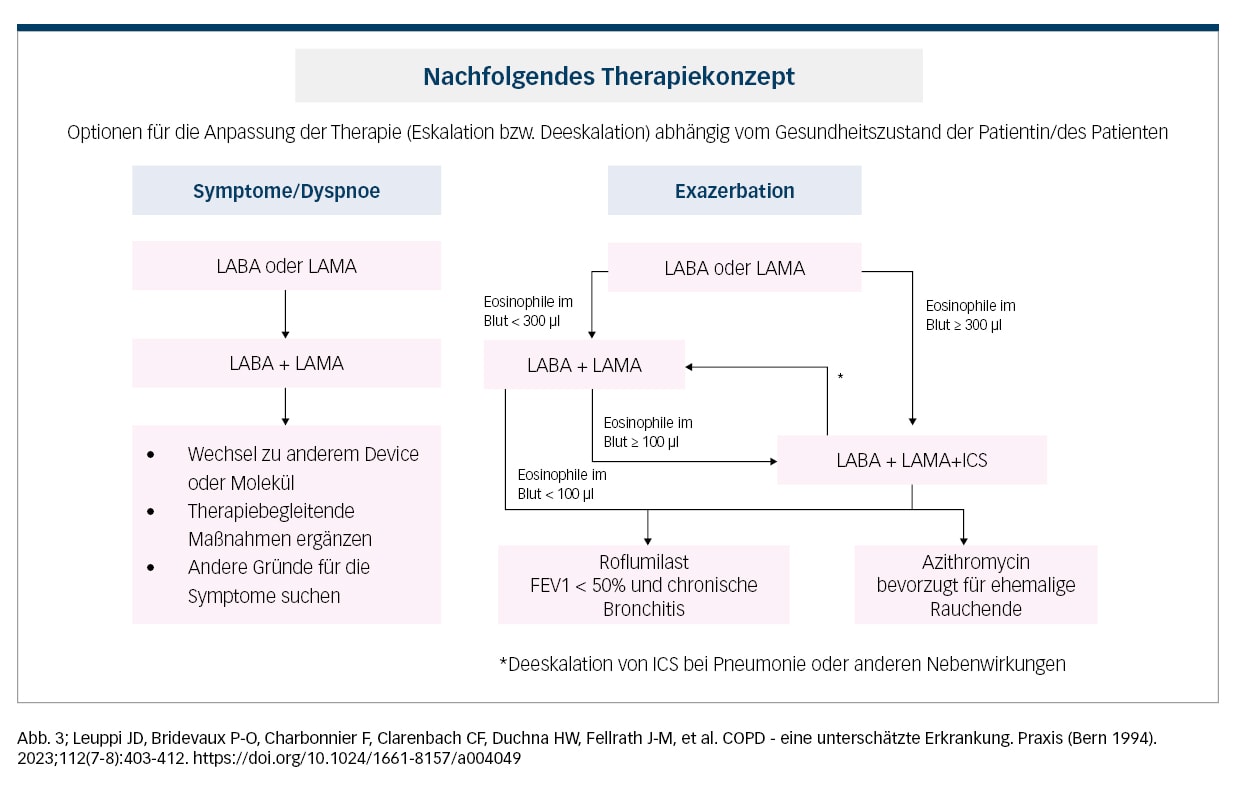
Erratum
Beim State of the Art-Artikel „COPD“, der in der ÖÄZ 1/2 vom 25. Jänner 2024 erschienen ist, ist es aufgrund eines technischen Problems zu einem Übertragungsfehler gekommen: Statt Eosinophile im Blut < 300 µl muss es richtig < 100 µl heißen. Wir bedauern! Die Redaktion
© Österreichische Ärztezeitung Nr. 3 / 10.02.2024